היסט סטוקס

היסט סטוקס הוא ההבדל (ביחידות אנרגיה, מספר גל או תדר) בין מיקומי המקסימום של ספקטרום הבליעה וספקטרום הפליטה של אותו מעבר אלקטרוני (כגון: פיזור רמאן ופלואורסצנציה).[1] המונח נקרא על שם הפיזיקאי האירי ג'ורג 'גבריאל סטוקס.[2][3][4] לעיתים היסטי סטוקס ניתנים ביחידות של אורך גל, אך יחידות אלו פחות משמעותיות מאשר יחידות אנרגיה, מספר גל או תדר מכיוון שהראשונות תלויות באורך גל הבליעה. לדוגמה, היסט סטוקס של 50 ננומטר מאורך גל בליעה של 300 ננומטר גדול יותר במונחי אנרגיה מאשר היסט סטוקס של 50 ננומטר מאורך גל בליעה של 600 ננומטר.
כאשר מערכת (בין אם מדובר במולקולה או באטום) בולעת פוטון, היא משיגה אנרגיה ונכנסת למצב מעורר. אחת הדרכים למערכת להגיע לרלקסציה היא פליטת פוטון שתגרום לאיבוד האנרגיה (שיטה אחרת היא אובדן האנרגיה כחום). כאשר לפוטון הנפלט יש פחות אנרגיה מהפוטון שנבלע, הבדל אנרגיה זה נקרא היסט סטוקס.
היסט סטוקס הוא בעיקר תוצאה של שתי תופעות: רלקסציה ויברציונית ורה-אורגניזצית ממס. פלואורופור הוא דיפול, המוקף מולקולות ממס. כאשר פלואורופור נכנס למצב מעורר, מומנט הדיפול שלו משתנה, אך מולקולות הממס שמסביב אינן יכולות להסתגל כל כך מהר. רק לאחר רלקסציה ויברציונית מומנטי הדיפול של המולקולות מסביב מתיישרים באותו כיוון.
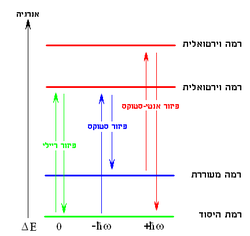
פיזור ריילי: פוטון מערר את המערכת למצב וירטואלי ונפלט ללא שינוי בתדירותו.
פיזור סטוקס: פוטון מערר את המערכת ממצב היסוד למצב וירטואלי ונפלט תוך איבוד אנרגיה מתאימה להפרש אנרגיות שני מצבים עצמיים.
פיזור אנטי-סטוקס: פוטון מערר את המערכת ממצב מעורר לרמה וירטואלית ונפלט תוך רכישת האנרגיה של המצב המעורר ביחס למצב היסוד.
פלואורסצנצית סטוקס
פלואורסצנצית סטוקס היא פליטה של פוטון באורך גל ארוך יותר (תדר או אנרגיה נמוכים יותר) על ידי מולקולה שבלעה פוטון באורך גל קצר יותר (תדר או אנרגיה גבוהים יותר).[5][6][7] גם בליעת אנרגיה וגם קרינה (פליטה) של אנרגיה ייחודיים למבנה מולקולרי מסוים. אם לחומר יש פער פסים ישיר בטווח האור הנראה, האור שזוהר עליו נבלע, מה שמעורר אלקטרונים למצב בעל אנרגיה גבוהה יותר. האלקטרונים נשארים במצב מעורר במשך כ- שניות. מספר זה משתנה על פי כמה סדרי גודל, תלוי בדגימה, ומכונה זמן חיים פלואורסצנטי של דגימה. לאחר איבוד כמות קטנה של אנרגיה באמצעות רלקסציה ויברציונית, המולקולה חוזרת למצב היסוד, ואנרגיה נפלטת.
היסט אנטי-סטוקס
אם לפוטון הנפלט יש יותר אנרגיה מהפוטון שנבלע, ההבדל באנרגיה נקרא היסט אנטי-סטוקס.[8] אנרגיה נוספת זו באה מפיזור פונונים תרמיים בסריג גבישי, שגורמים לקירור הגביש בתהליך. איטריום סולפיד-חמצני מזוהם עם גדוליניום סולפיד-חמצני הוא פיגמנט אנטי סטוקס תעשייתי נפוץ, בולע בתחום האינפרא אדום ופולט בתחום הנראה של הספקטרום. המרת פוטון עילית (Photon upconversion) היא תהליך אנטי-סטוקס נוסף. דוגמה לתהליך זה מודגם על ידי המרת ננו-חלקיקים עילית (Upconverting nanoparticles) הנפוצה יותר בספקטרוסקופיה של רמאן, שם ניתן להשתמש בה כדי לקבוע את הטמפרטורה של חומר.[9]
ראו גם
הערות שוליים
- ↑ Gispert, J. R, Coordination Chemistry, Wiley-VCH, 2008
- ↑ Albani, J. R., Structure and Dynamics of Macromolecules: Absorption and Fluorescence Studies, אלסביר, 2004
- ↑ Lakowicz, Joseph R. (1999). Principles of Fluorescence Spectroscopy. Kluwer Academic / Plenum Publishers. מסת"ב 978-0-387-31278-
- ↑ Guilbault, G.G. 1990. Practical Fluorescence, Second Edition, Marcel Dekker, Inc., New York.
- ↑ Banwell C.N. and McCash E.M. Fundamentals of Molecular Spectroscopy (4th ed., McGraw-Hill 1994) p.101 and p.113
- ↑ Atkins P . and de Paula J, Physical Chemistry, 8.0 ed, W.H. Freeman, 2006
- ↑ Rost, F. W. D., Fluorescence Microscopy, הוצאת אוניברסיטת קיימברידג', 1992
- ↑ Kitai, A., Luminescent Materials and Applications, John Wiley and Sons, 2008
- ↑ Keresztury, Gábor, Raman Spectroscopy: Theory". Handbook of Vibrational Spectroscopy, Chichester: Wiley, 2002
שגיאות פרמטריות בתבנית:מיון ויקיפדיה
שימוש בפרמטרים מיושנים [ דרגה ] היסט סטוקס27194413
