מעכבי משאבות פרוטונים
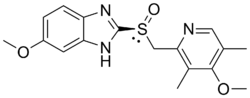
מעכבי משאבות פרוטונים או מעכבי משאבות מימן (באנגלית: Proton pump inhibitors; PPI) הם קבוצה של תרופות שפעולתן העיקרית היא הפחתה ארוכת טווח של ייצור חומצת הקיבה (אנ'). קבוצת תרופות זו יעילה בעיכוב הפרשת חומצה, והיא לעיתים קרובות מחליפה קבוצת תרופות שקדמה לה אנטגוניסטים ל-H2. רוב התרופות בקבוצה זו הן נגזרות של בנזימידזול (Benzimidazole), על אף שקיימות גם תרופות שהן נגזרות של אימידזופירידין (Imidazopyridine) שלהן תכונות שונות במקצת.[1] תרופות אלו הן בין התרופות הנמכרות ביותר, ונחשבות בטוחות יחסית, אולם צריכת ריכוזים גבוהים או שימוש ארוך טווח במעכבי משאבות פרוטונים עלול להעלות את הסיכוי לשבירת עצם.[2][3]
קיימים מעכבי משאבות פרוטונים רבים ביניהם אומפרזול, לנסופרזול, דקסלנסופרזול (Dexlansoprazole), אזומפרזול (Esomeprazole), פנטופרזול (Pantoprazole) ורבפרזול (Rabeprazole).
| מעכבי משאבות פרוטונים | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| שם גנרי בעברית | שם באנגלית | שמות מסחריים | מינונים עיקריים במ"ג | |||||||
| אומפרזול | Omeprazole | אומפרדקס | Omepradex | אומפרה | Omepra | 10 | 20 | 40 | ||
| אסומפרזול | Esomeprazole | נקסיום | Nexium | אסופרים | Esoprim | סולזול | Solezol | 20 | 40 | |
| פנטופרזול | Pantoprazole | קונטרולוק | Controloc | פנטואבניר | Pantoavenir | אולסרון | Ulceron | 20 | 40 | |
| לנסופרזול | Lansoprazole | לנטון | Lanton | לנסו | Lanso | 15 | 30 | |||
| דקסלנסופרזול | Dexlansoprazole | דקסילנט | Dexilant | 30 | 60 | |||||
| רבפרזול | Rabeprazole | אסיפקס | Aciphex | פריאט | Pariet | 10 | 20 | |||
התוויה
שימוש במעכבי משאבות פרוטונים עשוי להיעשות במסגרת טיפול בבעיות שונות ביניהן: דיספפסיה, כיב פפטי (אולקוס), רפלוקס קיבתי ושטי (צרבת), laryngopharyngeal reflux, תסמונת בארט, מניעת דלקת רפידת הקיבה, סינדרום זולינגר-אליסון, גסטרינומה ומצבים אחרים שבהם יש הפרשת יתר של חומצה.
יעילותו של הטיפול במעכבי משאבת מימן לא נבחן בכל אחד מהמקרים, על אף השימוש הנרחב שנעשה בהם במצבים אלו. כך למשל מעכבי משאבת מימן לא משנים את אורכה של תסמונת ברט.[4] הבדיקה המקובלת להערכת הצלחת הטיפול במעכבי משאבת מימן בחולי רפלוקס קיבתי ושטי היא ניטור חומציות ושט. ה-FDA ממליץ על לא יותר מ-3 סדרות טיפול של 14 יום בשנה.[2]
תופעות לוואי
באופן כללי נחשבים מעכבי משאבת מימן כתרופות בטוחות ותופעות לוואי בטווח הקצר הן נדירות למדי.[דרוש מקור] תופעות הלוואי השכיחות (עד 1 מ-10 מטופלים) הן כאב ראש, בחילה, שלשול, כאב בטן, עייפות, סחרחורת, פוליפים שפירים בקיבה.[5] בשימוש ארוך טווח תופעת לוואי אפשרית היא חסר מגנזיום בדם.[6]
תופעות לוואי נדירות כוללות פריחה, גירוד, עצירות, חרדה ודיכאון. מאחר שהגוף משתמש בחומצת הקיבה לפירוק B12 מהמזון, שימוש ארוך טווח במעכבי משאבת מימן עלול לגרום להפחתת הספיגה של הוויטמין ועלול להביא למצב של חסר בוויטמין B12. במקרים נדירים מאוד תופעות הלוואי של התרופות עשויות להיות דלקת של הרקמה האינטרסטיציאלית בכליות (interstitial nephritis), היפונתרמיה, היפוקלמיה, דלקת לבלב וסינדרום סטיבן-ג'ונסון.[7]
נמצא כי הפחתת החומצה הקיבתית באמצעות אנטגוניסטים ל-H2 ומעכבי משאבות מימן קשורה לעלייה בתחלואה בדלקת ריאות. הסבר שהוצע לכך היה שהפחתת חומציות הקיבה מתבטאת בהפחתת ההגנה מאורגניזמים פתוגניים, ומסיבה זו הוצע לרשום תרופות אלו לחולים שיש להם סיכון גבוה לדלקת ריאות רק במנות קטנות ורק כשהן הכרחיות.[8]
שימוש ארוך טווח במעכבי משאבות מימן נחקר פחות. במחקר שנעשה על 135,000 בני 50 או יותר, נמצא כי היה סיכוי גבוה פי 2.6 לשבירת ירך למטופלים שנטלו את התרופה במשך יותר משנה. אלו שנטלו את התרופה במנות מופחתות במשך שנה עד 4 שנים היו עם סיכון של פי 1.2 עד 1.6 לשבירת הירך. הסיכוי לשבר עולה עם משך הטיפול בתרופה.[9] תאוריות באשר לסיכוי המוגבר הן שהפחתת החומצה בקיבה מפחיתה את כמות הסידן שנספג בקיבה או שמעכבי משאבות מימן פוגעים בהרס ובבנייה מחדש של עצמות על ידי פגיעה באוסטאוקלסטים.
מחקר שבוצע בקרב מקבלי טיפול ארוך טווח עבור קיבה נגועה בחיידקי הליקובקטר פילורי מצא קשר לפיתוח סרטן הקיבה אצל משתמשי תרופות מקבוצת PPI לעומת משתמשי תרופות מקבוצת H2.[10] לפיכך נטען לסיכון גבוה בנטילת תרופות אלו, המשמשות גם כטיפול מקובל נגד צרבת. בשנה בה פורסם המחקר, 2017, טען משרד הבריאות הבריטי כי הסיכון נמוך וכי יש לקחת את תוצאות המחקר בפרופורציה הנכונה.[11] ב-2022 פורסם מחקר דומה, שמצא עליה בסיכון מוחלט לסרטן קיבה של כ-1 לכל 1200 איש שטופלו לאורך 10 שנים ב-PPI.[12]
מנגנון פעולה
מעכבי משאבות פרוטונים פועלים כמעכבים בלתי הפיכים למערכת אנזימי משאבת מימן-אשלגן (H+/K+ ATPase או משאבות פרוטונים) של תאי הדופן בקיבה. משאבות הפרוטונים הם השלב הסופי בהפרשת החומצה הקיבתית, והם אחראיים באופן ישיר להפרשת יוני H+. יכולתם להשפיע על שלב הסופי של ייצור החומצה, כמו גם טבעו הבלתי הפיך של העיכוב (הכוונה היא לאנזים הבודד, ההשפעה על מערכת העיכול כולה היא הפיכה), הופכים את מעכבי משאבות הפרוטונים למשפחת תרופות יעילות בהרבה מאנטגוניסטים ל-H2 והם מסוגלים להפחית את הפרשת החומצה הקיבתית בעד 99%.
הפחתת החומצה בקיבה מסייעת לריפוי כיבים בתריסריון, ומפחית את הסבל מצרבת ומהפרעות בעיכול, אשר יכולים להחמיר עם החומצה בקיבה. עם זאת מצב של מעט חומצה בקיבה נקרא גם היפוכלורידריה, ובו אין או שיש כמות מועטה של חומצת מימן כלורי, החיונית לפירוק חלבונים ולספיגת חומרים מזינים, במיוחד של ויטמין B12 וסידן.
מעכבי משאבות פרוטונים ניתנים כשהם בצורתם הבלתי פעילה הליפופילית. הם חוצים את קרום התא אל חלקים בתוך התא שבהם יש סביבה חומצית. בסביבה החומצית הם מקבלים פרוטונים, והופכים לצורתם הפעילה, הנקשרת קוולנטית ובאופן בלתי הפיך למשאבות הפרוטונים הקיבתיות, וגורמים בכך להשבתתן.
היסטוריה

בשנת 1975 התגלה על ידי מחלקת Hässle בחברת התרופות Astra בגטבורג בשוודיה[13] כי טימופרזול מעכב הפרשת חומצה ללא תלות בסוג הגירוי, בין אם תוך תאי או חוץ תאי[14]. מחקרים שנעשו על טימופרזול גילו הגדלה של בלוטת התריס עקב עיכוב של קליטת יוד כמו גם ניוון של התימוס. חיפוש בספרות העלה כי ישנן התמרות של מקרפטו-בנזימידזול שלהן אין השפעה על קליטת יוד והכנסת כמה מתמירים כאלו לטימופרזול הביאו לתרכובת ללא השפעות טוקסיות, ומבלי לפגוע בהשפעות החיוביות של הפחתת הפרשת חומצה. אומפרזול, נגזרת של טימופרזול, התגלה ב-1979, והיה לראשון בסדרה של תרופות השולטות על הפרשת חומצה בקיבה, מעכבי משאבות פרוטונים.
ב-1980 נכנסה התרופה לשימוש מוגבל כתרופה חדשה (Investigational New Drug), וב-1982 נכנסה התרופה לשלב השלישי בניסוי הקליני. גישה חדשה לטיפול במחלות הקשורות לחומצה נכנסה לשימוש, ואומפרזול הוכיחה תוך זמן קצר עדיפות קלינית על פני אנטגוניסטים לקולטני H2. ב-1988 החל שיווק של אומפרזול בשם לוסק (Losec®) באירופה וב-1990 בארצות הברית בשם פרילוסק (Prilosec®). ב-1996 הייתה לוסק לאחת התרופות הנמכרות בעולם, וב-2004 למעלה מ-800 מיליון איש טופלו בתרופה ברחבי העולם. במהלך שנות השמונים כ-40 חברות תרופות אחרות נכנסו לתחום התרופות המבוססות של עיכוב משאבות פרוטונים, אולם רק מעטות זכו להצלחה מסחרית: טקדה עם לנסופרזול, Byk Gulden עם פנטופרזול, וחברת התרופות Eisai עם רבפרזול - כולן תרופות אנלוגיות לאומפרזול.
קישורים חיצוניים
- מעכבי משאבות פרוטונים, באתר אנציקלופדיה בריטניקה (באנגלית)
הערות שוליים
- ↑ Sachs G, Shin JM, Howden CW (2006). "Review Article: The clinical pharmacology of proton pump inhibitors". Ailment. Pharmacol. Ther. 23 (2): 2–8. doi:10.1111/j.1365-2036.2006.02943.x.
{{cite journal}}: תחזוקה - ציטוט: multiple names: authors list (link) - ^ 2.0 2.1 "Possible Increased Risk of Bone Fractures With Certain Antacid Drugs". U S Food and Drug Administration. 25 במאי 2010.
{{cite web}}: (עזרה) - ↑ תרופות מסוג מעכבי משאבת מימן וחסמי H2 קשורות לסיכון לשבר בעצם הירך (מתוך כנס של Digestive Disease Week), באתר e-med
- ↑ Cooper BT, Chapman W, Neumann CS, Gearty JC (2006). "Continuous treatment of Barrett's oesophagus patients with proton pump inhibitors up to 13 years: observations on regression and cancer incidence". Aliment. Pharmacol. Ther. 23 (6): 727–33. doi:10.1111/j.1365-2036.2006.02825.x. PMID 16556174.
{{cite journal}}: תחזוקה - ציטוט: multiple names: authors list (link) - ↑ מאגר התרופות - נקסיום, באתר israeldrugs.health.gov.il
- ↑ Proton Pump Inhibitor drugs (PPIs): Drug Safety Communication - Low Magnesium Levels Can Be Associated With Long-Term Use, באתר ה-FDA
- ↑ Long-term management of patients taking proton pump inhibitors
- ↑ Laheij RJF, Sturkenboom MCJM, Hassing R-J, Dieleman J, Stricker BHC, Jansen JBMJ. Risk of community-acquired pneumonia and use of gastric acid-suppressive drugs. JAMA 2004;292(16): 1955-60. PMID 15507580
- ↑ Yang, YX; Lewis JD; Epstein S; Metz DC (27 דצמ' 2006). "Long-term proton pump inhibitor therapy and risk of hip fracture". Journal of the American Medical Association. 296 (24): 2947–53. doi:10.1001/jama.296.24.2947. PMID 17190895.
{{cite journal}}: (עזרה) - ↑ Ka Shing Cheung, Esther W. Chan, Angel Y. S. Wong, Lijia Chen, Long-term proton pump inhibitors and risk of gastric cancer development after treatment for Helicobacter pylori: a population-based study, Gut, 2017-09-18, עמ' gutjnl–2017–314605 doi: 10.1136/gutjnl-2017-314605
- ↑ (NHS Choices: Behind the Headlines - Acid reflux drugs linked to increased stomach cancer risk בארכיון Wayback Machine (אורכב 07.11.2017))
- ↑ Devin Abrahami, Emily Gibson McDonald, Mireille E. Schnitzer, Alan N. Barkun, Samy Suissa, Laurent Azoulay, Proton pump inhibitors and risk of gastric cancer: population-based cohort study, Gut 71, 2022-01, עמ' 16–24 doi: 10.1136/gutjnl-2021-325097 (באנגלית)
- ↑ Lars Olbe, Proton pump inhibitors, Birkhäuser 1999. p. 41 מסת"ב 3764358971
- ↑ Sachs G, Shin JM, Vagin O, Lambrecht N, Yakubov I, Munson K. (July 2007), The Gastric H,K ATPase as a Drug Target, Journal of Clinical Gastroenterology
מעכבי משאבות פרוטונים40519533Q421704
